Schutzrechte bei Fertigarzneimitteln sind ein komplexes Thema, das
pharmazeutische Anbieter im schlimmsten Fall ordentlich Geld kosten
kann: Wer hier nicht genau Bescheid weiß und unwissentlich Rechte
verletzt, wird vom Staat zur Kasse gebeten. Deshalb versuchen viele
Unternehmen mit den öffentlich zugänglichen Datenbanken die Brands
und Verfahrensstati ihrer Wirkstoffe im Blick zu behalten.
Schließlich gilt es bei bestehenden und auslaufenden Schutzrechten
bestens informiert zu sein, um den Lebenszyklus eigener und fremder
Produkte optimal zu planen. Doch immer wieder zeigen sich diese
öffentlichen Datenbanken als beinahe unüberwindbares Hindernis, wenn
abweichende Bezeichnungen oder Schreibfehler die Recherche
erschweren. Auch ein sicherer Umgang mit dem Unterlagenschutz ist für
pharmazeutische Anbieter längst essentiell und fordert insbesondere
bei der Arbeit mit öffentlichen Recherchedatenbanken weit mehr als
nur fachliches Know-How: Die Schutzrechte von Fertigarzneimitteln
sind ein dichtes Geflecht aus den unterschiedlichsten
Familienbeziehungen. Denn aus vielen Grundpatenten entstehen
unmittelbar weitere Schutzzertifikate mit unterschiedlich langen
Laufzeiten. Diese Laufzeiten einzelner Schutzzertifikate können sich
wiederum ungewollt verkürzen, vorzeitig erlöschen oder aber
verlängern, z.B. durch einen Antrag auf Kinderarzneimittel.
Obwohl diese Zertifikate so eng verflochten sind, genügt auf der
Seite des DPMA® (Deutsches Patent- und Markenamt) in den seltensten
Fällen allein der Wirkstoffname für eine erfolgreiche Recherche:
Neben abweichender Bezeichnungen (beispielsweise bei Indikationen)
können auch Schreibfehler, chemische Formeln, abweichende
Schreibweisen, die Nennung von Wirkstärken oder gar ein
Inhaberwechsel zu schlechter Erkennbarkeit und Interpretationsfehlern
führen. Deshalb ist dieser wertvolle aber komplexe Datenbestand kaum
maschinell auslesbar oder in Anschlusssystemen weiter zu verwenden.
Um die gewonnenen Informationen tatsächlich nutzbar zu machen, ist
häufig hoher Personalaufwand nötig.
Eine Lösung für dieses Problem bietet nun PSE – Pharma Solutions
Europe mit der PSE-Patentschutzdatenbank®. Das Unternehmen ist seit
Jahren als Spezialanbieter in der Pharmaindustrie etabliert und hat
es sich zur Aufgabe gemacht, den Datendschungel für pharmazeutische
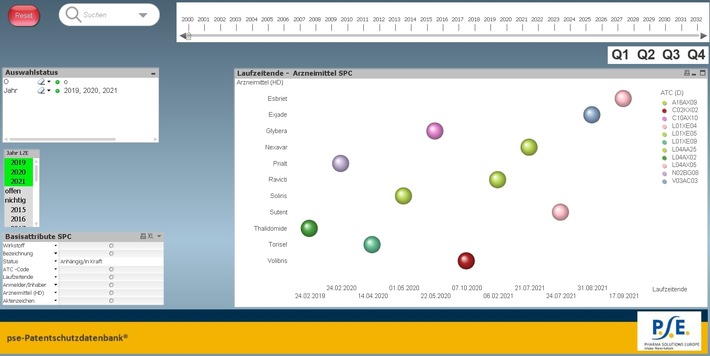
Anbieter zu lichten: Mit der PSE-Patentschutzdatenbank® können
innerhalb verkürzter Zeit zielgenauere Analysen zu Schutzrechten bei
Arzneimitteln durchgeführt werden.
Die Besonderheit: Durch die integrierten Suchpfade lassen sich
auch die Schutzrechtssituationen einzelner Teilmärkte, Produkte,
Anmelder und Inhaber je nach Zeitraum des Ablaufdatums per Mausklick
anschaulich darstellen. Auch die Kriterien „Orphan Drug“,
„Impfstoffe“, „Tierarzneimittel“ und „Kinderarzneimittel“ können als
Filter gesetzt werden. Die Aktualisierungs- und Clearingfrequenzen
der PSE-Patentschutzdatenbank® sind kundenorientiert engmaschig
getaktet und finden wöchentlich zeitnah zu den
Donnerstags-Publikationen des DPMA® statt.
Dabei werden sämtliche Verfahrensstände nach Art berücksichtigt:
– Zertifikatsanmeldungen
– Erteilte oder zurückgewiesene Zertifikate
– Bewilligte oder zurückgewiesene Anträge auf Verlängerung der
Laufzeit
– Anträge auf Berichtigung oder Widerruf der Laufzeit
– Zurückgenommene Zertifikatsanträge
– Erloschene oder nichtige Zertifikate
– Wiedereinsetzungen
Damit bietet PSE – Pharma Solutions Europe einen Service, den man
bereits auch außerhalb der Grenzen Europas zu schätzen weiß. Auch in
der Türkei heißt man diese neue Möglichkeit zur Analyse von
Schutzrechten willkommen, bietet sie doch eine wichtige Hilfestellung
gerade im Bereich der Orphan Drugs. Diese Medikamente, die in der
Behandlung gegen seltenere Krankheiten eingesetzt werden, sind hier
von großer Bedeutung für die Volksgesundheit: Aufgrund der häufigeren
Eheschließung zwischen nahen Angehörigen ist in der Türkei die Zahl
der seltenen Krankheiten, die vererbt oder rezessiv vererbt werden,
im Vergleich zu Europa und der USA deutlich höher. (Man spricht von
rund 7 Millionen Fällen in der Türkei (Quelle: mynet.com, 13.08.2018)
und knapp 4,3 Millionen in Deutschland, bei vergleichbarer
Einwohnerzahl (Quelle: Pharmazeutische Zeitung Online, 13.08.2018)).
Da jedoch im Bereich Orphan Drugs kaum ein „Return on Investment“
möglich ist, weigern sich pharmazeutische Unternehmen in der Türkei
diese Medikamente zu den gängigen Marktbedingungen zu entwickeln.
Deshalb wurden 2017 vom türkischen Gesundheitsministerium neue
Richtlinien implementiert, die Firmen beim Marktzugang in diesem
Bereich unterstützen: Orphan-Drug-Identification-Anträge sind
mittlerweile kostenfrei und selbst bei der Produktion tragen
Unternehmen lediglich noch 10% der Kosten selbst. Diese Entwicklung
hat nun zur Folge, dass sich zahlreiche türkische Unternehmen nach
möglichen Mitvertriebsrechten auch deutscher Unternehmen umschauen,
deren Wirkstoffe entweder kein wirksames Schutzzertifikat mehr
besitzen, bei denen noch aktive Schutzrechte vorhanden sind oder die
sich im Verfahrensstatus befinden, eine Anerkennung als besonders
schutzwürdig zu erhalten.
Diese Suche nach Mitvertriebsrechten wird durch die integrierten
Suchpfade der PSE-Patentschutzdatenbank® auf Anschlussdatenbanken
europäischer Zulassungsbehörden merklich erleichtert. Damit
revolutioniert PSE – Pharma Solutions Europe für deutsche Unternehmen
den Umgang mit Schutzrechten.
Pressekontakt:
LeonARTo.de
Carina Bukenberger
Wolfgang-Stock-Straße 14
72076 Tübingen
www.LeonARTo.de
info@LeonARTo.de
+49 157 51151995
Original-Content von: PSE – Pharma Solutions Europe, übermittelt durch news aktuell